Ozono.
¿Qué es el Ozono?
El ozono (O3) es una molécula triatómica formada por átomos de oxígeno. Es un alótropo del oxígeno mucho más reactivo que el oxígeno diatómico (O2). Es un poderoso oxidante que reacciona rápidamente con otros compuestos químicos, es inestable cuando se encuentra en altas concentraciones. Bajo condiciones atmosféricas normales, el ozono decae a oxígeno diatómico en un lapso de aproximadamente 30 minutos. En 1840, el químico alemán Christian Friedrich Schönbein le dio el nombre de ozono, de la raíz griega ozein (olor), debido a su olor característico.

fuente: http://www.ozononet.com/wp-content/uploads/2015/09/molecula_ozono1.png
¿Dónde se encuentra?
El ozono es un componente natural de la atmósfera que se encuentra en bajas concentraciones y es vital para la vida. La mayor parte del ozono se encuentra en la parte superior de la atmósfera en una región de la estratósfera, a más de 20 km de la superficie, llamada ozonósfera en donde se concentra más del 90% del ozono atmosférico y forma una capa que limita el ingreso de radiación ultravioleta proveniente del Sol.
La capa de ozono.
Alrededor del 90% de todas las moléculas del ozono residen en la estratósfera en una región definida conocida como ozonósfera, a una altitud entre 20 y 30 km. Esta región también se conoce como capa de ozono. La capa de ozono evita que los peligrosos rayos ultravioleta lleguen a la superficie de la Tierra. El ozono absorbe longitudes de onda menores a 345 nanómetros (nm), también absorbe débilmente longitudes de onda entre 450 y 750 nm. En 1974 Molina y Rowland demostraron que los compuestos antropogénicos clorados pueden destruir la capa de ozono. Desde finales de los 70 la reducción de la capa de ozono se relaciona directamente con el incremento en la concentración de cloro y bromo en la atmósfera.

fuente: http://necesitodetodos.org/wp-content/uploads/2014/11/ozono.jpg
El ozono estratosférico.
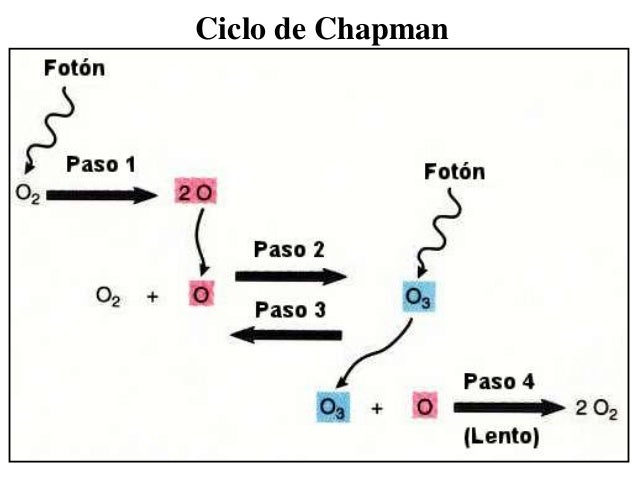
El ozono desempeña un papel central en la química atmosférica, además de ser un gas altamente reactivo, es capaz de absorber luz infrarroja y ultravioleta, contribuyendo al efecto invernadero y proporcionando protección contra la luz ultravioleta del Sol. La fotoquímica de la producción del ozono en la estratósfera es similar a la que ocurre en la tropósfera, excepto que el ozono estratosférico se produce después de la fotólisis del oxígeno molecular, mientras que en la tropósfera se produce después de la fotólisis del dióxido de nitrógeno. En 1930 el físico inglés Sydney Chapman sugirió que la fotólisis del oxígeno molecular era la responsable de la formación del ozono en la estratósfera y propuso las reacciones fundamentales de formación-destrucción de ozono, estas reacciones se conocen como el ciclo de Chapman:
fuente: http://image.slidesharecdn.com/unidad2parte2-150108155523-conversion-gate01/95/unidad-2-parte-2-22-638.jpg?cb=1420732605000
De manera general, la formación del ozono en la estratósfera ocurre en un proceso de dos pasos. En el primero, la luz ultravioleta rompe fotolíticamente una molécula de oxígeno (O2), separándola en dos átomos de oxígeno (O). En el segundo, cada átomo de oxígeno colisiona con otra molécula de oxígeno para formar una molécula de ozono. El ozono formado puede separarse fotolíticamente por acción de la luz ultravioleta para generar una molécula de oxígeno y un átomo de oxígeno en estado excitado. Las mayores concentraciones de ozono ocurren en donde la radiación solar ultravioleta encuentra la cantidad suficiente de oxígeno, generalmente a una altitud de 25 a 32 km. La concentración de ozono disminuye gradualmente al descender en la tropósfera.
Ozono bueno y Ozono malo
En la atmósfera terrestre, el ozono puede ser “bueno” o
“malo” dependiendo de dónde se encuentre. El ozono “bueno” está en la
estratósfera (capa entre los 17 y 48 km de altura) y actúa como un filtro que
detiene la parte más perjudicial de la radiación ultravioleta proveniente del
sol. El “malo” está en la tropósfera (la región más próxima a la superficie
terrestre, hasta unos 17 km de altura). Es perjudicial para la salud de
animales y plantas.
El ozono “bueno” se forma a partir del oxígeno (O2) del
aire, por acción de la luz UV (ultravioleta). El proceso es reversible (el O3
se descompone lentamente a O2) y ocurre principalmente en la parte superior de
la estratósfera (30-45 km de altura) originando una capa (“capa de ozono”)
renovable y de una concentración que no varía porque la velocidad de formación
es igual a la de descomposición. La concentración de ozono varía con el lugar y
la época del año. Su concentración no es muy alta pero es vital para la vida
porque absorbe casi el 99% de la radiación UV tipo B (de 280-320 nm) que es la
responsable de mutaciones genéticas (cáncer de piel) y cataratas. Además,
debilita el sistema inmunológico y disminuye la fotosíntesis de las plantas.
Ozono malo, es el que se forma en la atmósfera inferior de
la Tierra, cerca del nivel del suelo, cuando los contaminantes emitidos por
automóviles, plantas generadoras de energía, calderas industriales, refinerías,
plantas químicas, y otras fuentes, reaccionan químicamente en la presencia de
la luz solar. Éste es el dañino para los humanos, e incluso para los animales.
La acción perjudicial del ozono “malo” fue descubierta en
1940 al hallarlo responsable del deterioro de neumáticos y artículos de goma
almacenados por mucho tiempo y, además, afectaba la vegetación. Los primeros en
percibir su efecto fueron los asmáticos que, hasta entonces, utilizaban aire
purificado con ozono. Son varias las fuentes que lo originan: una parte viene
de la estratósfera, al ser arrastrado por los vientos hacia la tropósfera. Otra
parte se origina por un complicado proceso químico en el que participan la luz
solar, el óxido de nitrógeno y una serie de compuestos orgánicos volátiles
(COV). Éstos provienen de procesos biológicos (de la vegetación, fermentación),
de los gases volcánicos y de emisiones de motores de vehículos e industrias.

Efectos en la salud por el ozono.
En el organismo el ozono ejerce su acción a través de varios
mecanismos. Las reacciones con algunas moléculas biológicas pueden llevar a la
formación de radicales libres. El ozono no puede penetrar a través de las
membranas celulares o las capas surfactantes de las células, por lo que sus
efectos biológicos pueden ser provocados por intermediarios tales como radicales
libres, aldehídos, peróxido de hidrógeno, entre otros. Cuando el tracto
respiratorio es expuesto al ozono se produce daño en el mismo, el alcance
dependerá de la concentración de ozono, la duración de la exposición, los
patrones de exposición y la ventilación. La limpieza mucociliar decrece por la
exposición aguda. Los macrófagos alveolares, responsables de la limpieza en la
región pulmonar y participantes en la respuesta inmune, pueden disminuir su
fagocitosis y su actividad metabólica antimicrobial, incrementar la liberación
de prostaglandinas y alterar su cantidad. Estos efectos aumentan la
susceptibilidad a las infecciones respiratorias. En asmáticos expuestos
diariamente al ozono, se ha reportado un incremento en la incidencia de ataques
asmáticos y síntomas respiratorios. El ozono reduce la función pulmonar y hace
más difícil la respiración profunda y vigorosa. Cuando esto sucede, la
respiración comienza a sentirse incómoda. Si se realiza ejercicio o trabajo al
aire libre, se puede notar una respiración más rápida y superficial de lo
normal. A concentraciones elevadas de ozono se puede agravar el asma, debido a
que el ozono favorece la susceptibilidad del organismo a los alérgenos (agentes
que provocan los ataques). Puede empeorar las enfermedades pulmonares crónicas
tales como el enfisema y la bronquitis y reducir la capacidad del sistema
inmunológico para defenderse de las infecciones bacterianas. El ozono puede
causar daño permanente al pulmón. El daño en el corto plazo por causa del ozono
en los pulmones de niñ@s en desarrollo, puede resultar en una función pulmonar
reducida en la edad adulta. En los adultos, la exposición al ozono puede
acelerar la disminución natural de la función pulmonar que ocurre como parte
del proceso normal de envejecimiento.

Alotropía
¿Qué es alotropía?
La alotropía es la cualidad de algunos elementos que en el mismo estado físico pueden presentarse con dos o mas estructuras diferentes, razón por la cual sus propiedades serán también diferentes.
Ejemplo:
Variedades alotrópicas del oxígeno
Oxígeno diatómico O2
|
Ozono O3
|
| 1. permite la combustión 2. Estable a condiciones ambientales 3. Apto para la respiración | 1. Absorbe la radiación ultravioleta 2. Se descompone lentamente en O2 a condiciones ambientales 3. Es tóxico, no es apto para la respiración |
Existen otros elementos que presentan formas alotrópicas, tales como el carbono (carbón, grafito,diamante, fullereno); azufre (amorfo,rómbico, monoclínico, plástico) fosforo (rojo y blanco).

carbono
No hay comentarios.:
Publicar un comentario